Инновационные лекарства охватывают несколько терапевтических областей, а затраты, время и риски, связанные с кандидатами, вступающими в клиническое развитие, значительно увеличиваются. Необходимо использовать рациональную стратегию исследований, в полной мере используя существующие технологии, концентрируя ресурсы на кандидатах с потенциалом развития и устранение тех, у кого нет жизнеспособного будущего, чтобы минимизировать отходы ресурсов на проектах, вряд ли достигнут успеха.
Нет простого, готового ответа о том, как смягчить риски клинического развития, повысить показатели успеха и ускорить одобрение безопасных и эффективных лекарств. Кроме того, исследовательские стратегии сильно различаются в разных терапевтических областях. Одним из наиболее оцененных подходов является использование проверки механистической и проверки концепции (POC) в исследованиях на ранней стадии. Руководства 2024 года для неклинических исследований генной терапии генной терапии аденоассоции (AAV), а также явно упоминают о важности POC. Но что именно подтверждено через POC?
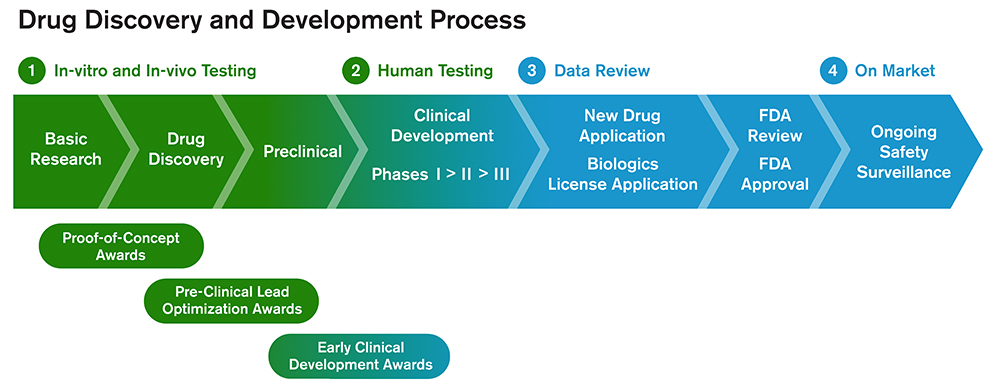
Генная терапия разработана на основе глубокого понимания механизмов заболевания и разработана для эффективного экспрессии в тканях или клетках -мишенях, связывается с сайтами -мишенями и модулирует их функцию для оказывания фармакологических эффектов, которые изменяют прогрессирование заболевания и приводят к клинической пользе. Эффекты вне цели считаются неблагоприятными. Процесс может быть кратко описан на следующих этапах: ① Препарат достигает целевых клеток. ② Препарат экспрессирует в клетках -мишенях и связывается с сайтом -мишенью. ③ Целевой сайт вызывает фармакологический эффект. ④ Этот эффект приводит к клинически значимым изменениям (терапевтические результаты).
Понимание механизма действия препарата в начале разработки помогает направлять дизайн и оптимизацию лекарств, что позволяет выбирать лучших кандидатов для дальнейшего развития. На более поздних этапах можно использовать методы для проверки механизма действий, закладывая основу для дальнейшего развития и, в конечном итоге, повышение уровня успеха и снижения рисков.
Доклиническое доказательство концепции (POC)включаетвне телаи исследования на животных, чтобы первоначально проверить, осуществляется ли терапевтическая стратегия на основе AAV, включая оценку эффективности и предварительной безопасности. Он знаменует собой критический переход от лабораторных исследований к доклиническому развитию (исследования токсикологии GLP).
Основные цели POC
- Утверждение научных гипотез: Проверка, может ли вектор AAV доставить целевой ген, независимо от того, экспрессируется ли он в тканях -мишенях, и может ли он улучшить фенотипы заболевания.
- Контроль риска: Выявление потенциальных проблем (например, иммуногенность, нецелевые эффекты), чтобы минимизировать риск неудачи во время более позднего развития.
- Оптимизация: Определение оптимальной конструкции вектора (серотип, промотор), маршрут введения и диапазон дозы.
Зачем нужен POC?
- Научная проверка: Убедитесь, что стратегии редактирования/замены генов эффективны в живых моделях и избегают ложных срабатываний, наблюдаемых в клеточных экспериментах. Убедитесь, что таргетирование тканей AAV соответствует ожиданиям (например, способность AAV9 пересекать гематоэнцефалический барьер).
- Снижение риска развития: Приблизительно 70% неудач разработки лекарств связаны с недостаточной эффективностью или проблемами токсичности на доклинических стадиях (Hature Reviews Deciply Decordy). POC помогает рано выйти из неэффективных стратегий.
- Поддержка приложений Ind: Данные POC являются ключевой ссылкой для регулирующих органов (например, FDA, EMA) для оценки обоснования клинических испытаний. Отсутствие POC может привести к отказу от инд.
- Привлечение инвестиций: Чистые результаты POC обеспечивают основу для финансирования и партнерских отношений, особенно в дорогостоящей области генной терапии.

Как внедрить POC?
Выбор цели и модели заболеваний
Механизм болезней: Понять, является ли это расстройством одного гена (например, гемофилия) или многофакторное заболевание (например, нейродегенеративные заболевания).
Модели нокаут/мутации (например,Ревматоидный артрит/ЦРУ).
Индуцированные модели (например,Стеатоз печени/ NASH/ MASH).
Валидация модельной патологии и сходства с болезнями человека имеет важное значение.
AAV Вектор Дизайн
- Выбор серотипа: Выберите на основе тканей -мишеней (например, AAV8 нацелен на печень, AAVRH10 для ЦНС).
- Оптимизация промоутера: Используйте тканевые промоторы (например, CTNT для миокарда) для усиления целевой экспрессии.
- Трансген дизайн: Включите оптимизацию кодонов и регуляторные элементы (например, WPRE для повышенной экспрессии).
Исследования in vitro
- Проверка линии ячейки: Эффективность трансдукции вектора тестирования, уровни экспрессии генов и токсичность в клетках HEK293 или первичных клетках.
- Анализ вне цели: Оценить непреднамеренные изменения с помощью RNA-seq или секвенирования всего генома.
- Маленькие животные in vivo исследования
- Административный маршрут: Внутривенная (системная доставка), локализованная (субретинальная) или внутримосферальная инъекция.
Маркеры эффективности
Биомаркеры (например, увеличение активности фактора коагуляции IX).
Функциональное восстановление (например, тестирование мышечной силы, поведенческие улучшения).
Гистологический анализ (например, иммуногистохимия для экспрессии целевого белка).
Разведка доза
Проверьте различные дозы, чтобы определить минимальную эффективную дозу (MED) и максимальную переносимую дозу (MTD).
Предварительная оценка безопасности
- Острая токсичность:Мониторинг веса, активности и биохимических маркеров сыворотки (например, ALT/AST).
- Иммуногенность: Оценка нейтрализующих антител против AAV и T-клеточных реакций (например, IFN-секреция Elispot).
- Векторное распределение: Используйте QPCR для оценки векторной ДНК в основных органах (печень, сердце, мозг, гонады).
Долгосрочное наблюдение
Следите за постоянством экспрессии генов (6-12 месяцев) и любого потенциального снижения с течением времени.
Ищите отложенную токсичность (например, фиброз печени, риски образования опухоли).
Вспомогательные стандарты для доклинических исследований
В опубликованных исследованиях Коэна обобщают три ключевых столпа, поддерживающие развитие кандидата на лекарство:
- Целевая экспозиция: Препарат должен достичь целевого участка.
- Целевая занятость: Препарат должен эффективно связываться с мишенью.
- Функциональное действие: Препарат должен вызывать функциональный эффект на цель.
Если эти три критерия соответствуют, вероятность успешной разработки лекарств является самой высокой. Если только некоторые из них встречаются или неудовлетворены, шансы на успех значительно снижаются. Для продуктов генной терапии AAV требуется дальнейшая уточнение этих критериев.
Ключевые факторы успеха
Значительные улучшения в конечных точках первичной эффективности (например, экспрессия белка, связанная с заболеванием, превышающую или равную 20% нормальной).
Репликация эффективности приводит к тому, что по крайней мере две модели (например, мыши + крупные животные).
Приемлемая безопасность
Нет тяжелой токсичности (например, печеночная недостаточность, нейровоспаление).
Контролируемые иммунные ответы (нейтрализующие титры антител<1:100 or manageable with immunosuppressive pretreatment).
Четкий диапазон дозы
Создайте MED и MTD и определите отношения дозы-ответа.
Четкий механизм действия
Подтвердите векторное биографическое распределение AAV и экспрессию трансгена в тканях -мишенях (например, с использованием визуализации in vivo или срезов тканей).
Воспроизводимость и стабильность
Independent production of AAV vectors in different batches, with consistent results and compliance with preliminary quality control standards (e.g., purity >90%, пустой капсид<20%).
Соображения
Ограничения животных моделей
Модели грызунов могут не полностью воспроизвести заболевания человека (например, различия иммунной системы), требуя проверки с крупными животными (свиньи,NHPS).
Регулирующие вариации
Руководства FDA (например, 2020 «Генная терапия человека при нейродегенеративных заболеваниях») может потребовать конкретных данных безопасности (например, репродуктивная токсичность).
Оценка ресурсов
В фазе POC баланс глубины исследований с затратами имеет решающее значение (например, использование трансгенных мышей может быть дороже, чем индуцированные модели).
Заключение
Доклинический POC является основным компонентом развития генной терапии AAV, требующей систематической проверки эффективности и безопасности при оптимизации параметров лечения. Критерии успеха включают в себя воспроизводимые данные о эффективности, контролируемую риски токсичности и четкие отношения доза-ответа, в конечном итоге закладывая основу для применений IND и клинических испытаний.












